Respostas
-
Resposta Questão 1
Alternativa “b”.
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2
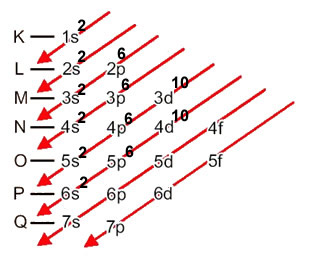
Distribuição eletrônica do bário no diagrama de Pauling
-
Resposta Questão 2
Alternativa “d”.
A distribuição eletrônica do titânio em ordem energética crescente é: 1s2 2s2 2p6 3s2 3p6 4s23d2. Portanto, o seu subnível mais energético é o último a ser preenchido: 3d2:
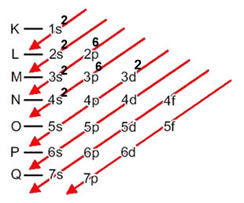
Distribuição eletrônica do titânio no diagrama de Pauling
Apenas para tirar quaisquer dúvidas, o subnível 4s2 é o mais externo e não o mais energético.
-
Resposta Questão 3
Alternativa “e”.
Pelo diagrama mostrado logo mais abaixo, você poderá ver que em cada camada a quantidade de elétrons é:
1ª camada: K = 2;
2ª camada: L = 8;
3ª camada: M = 14;
4ª camada: N = 2;
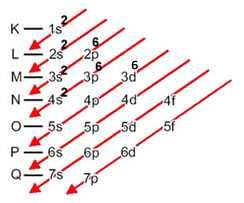
Distribuição eletrônica do ferro
-
Resposta Questão 4
Alternativa “d”.
O 3º nível energético é M, então, basta realizar a distribuição eletrônica, seguindo a ordem dada pelas setas, até que haja 14 elétrons nesse nível (2 + 6 + 6):

Distribuição eletrônica de 14 elétrons no terceiro nível do diagrama de Pauling
Somando todos os elétrons distribuídos, temos que o total é igual a 26.
-
Resposta Questão 5
Alternativa “c”.
O nível M é o terceiro, então, se olharmos esse nível, temos que os orbitais 3s e 3p estão preenchidos com elétrons, restando os 5 vazios do subnível 3d:
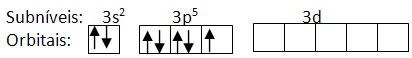
Subníveis e orbitais do nível M
-
Resposta Questão 6
Alternativa “b”.
Pela distribuição eletrônica mostrada no enunciado (1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s24d1), vemos que os elétrons foram distribuídos até a camada 5 (5s2). Visto que essa distribuição já está na ordem energética crescente, o subnível mais energético é o 4d que possui 1 elétron.
Resposta Questão 1
Alternativa “b”.
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2

Distribuição eletrônica do bário no diagrama de Pauling
Resposta Questão 2
Alternativa “d”.
A distribuição eletrônica do titânio em ordem energética crescente é: 1s2 2s2 2p6 3s2 3p6 4s23d2. Portanto, o seu subnível mais energético é o último a ser preenchido: 3d2:

Distribuição eletrônica do titânio no diagrama de Pauling
Apenas para tirar quaisquer dúvidas, o subnível 4s2 é o mais externo e não o mais energético.
Resposta Questão 3
Alternativa “e”.
Pelo diagrama mostrado logo mais abaixo, você poderá ver que em cada camada a quantidade de elétrons é:
1ª camada: K = 2;
2ª camada: L = 8;
3ª camada: M = 14;
4ª camada: N = 2;
2ª camada: L = 8;
3ª camada: M = 14;
4ª camada: N = 2;

Distribuição eletrônica do ferro
Resposta Questão 4
Alternativa “d”.
O 3º nível energético é M, então, basta realizar a distribuição eletrônica, seguindo a ordem dada pelas setas, até que haja 14 elétrons nesse nível (2 + 6 + 6):

Distribuição eletrônica de 14 elétrons no terceiro nível do diagrama de Pauling
Somando todos os elétrons distribuídos, temos que o total é igual a 26.
Resposta Questão 5
Alternativa “c”.
O nível M é o terceiro, então, se olharmos esse nível, temos que os orbitais 3s e 3p estão preenchidos com elétrons, restando os 5 vazios do subnível 3d:

Subníveis e orbitais do nível M
Resposta Questão 6
Alternativa “b”.
Pela distribuição eletrônica mostrada no enunciado (1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s24d1), vemos que os elétrons foram distribuídos até a camada 5 (5s2). Visto que essa distribuição já está na ordem energética crescente, o subnível mais energético é o 4d que possui 1 elétron.
Nenhum comentário:
Postar um comentário